 (April 2024) Die elektronische Patientenakte (kurz: ePA) hat seit ihrer Einführung zum 01.01.2021 in Deutschland viel Aufmerksamkeit erregt. Eine neue Studie, durchgeführt von der Ernst-Abbe-Hochschule Jena, untersucht die Einstellungen und Präferenzen der Bevölkerung zur ePA sowie die Bereitschaft, Gesundheitsdaten für medizinische Forschungszwecke zur Verfügung zu stellen. Weiterlesen
(April 2024) Die elektronische Patientenakte (kurz: ePA) hat seit ihrer Einführung zum 01.01.2021 in Deutschland viel Aufmerksamkeit erregt. Eine neue Studie, durchgeführt von der Ernst-Abbe-Hochschule Jena, untersucht die Einstellungen und Präferenzen der Bevölkerung zur ePA sowie die Bereitschaft, Gesundheitsdaten für medizinische Forschungszwecke zur Verfügung zu stellen. Weiterlesen
Digitale Gesundheit in Deutschland: Ausgabe des Bundesgesundheitsblatts beleuchtet Zukunftsperspektiven
 (April 2024) In der jüngsten Ausgabe des Bundesgesundheitsblatts steht die digitale Transformation im Gesundheitswesen im Mittelpunkt. Unter dem Titel „Digitale bevölkerungsbezogene Gesundheit in Deutschland – Beispiele aus der Forschung im Leibniz Wissenschafts-Campus Digital Public Health“ werden wegweisende Beiträge präsentiert, die das Potenzial digitaler Technologien für die öffentliche Gesundheit ausleuchten. Weiterlesen
(April 2024) In der jüngsten Ausgabe des Bundesgesundheitsblatts steht die digitale Transformation im Gesundheitswesen im Mittelpunkt. Unter dem Titel „Digitale bevölkerungsbezogene Gesundheit in Deutschland – Beispiele aus der Forschung im Leibniz Wissenschafts-Campus Digital Public Health“ werden wegweisende Beiträge präsentiert, die das Potenzial digitaler Technologien für die öffentliche Gesundheit ausleuchten. Weiterlesen
Ingo Nöhr und Kumpel Jupp, Kolumne: Folge 9 „Was gibt es Neues im Gesundheitswesen?“
 (April 2024) Bereits vor zehn Jahren machte sich unser Duo Gedanken über eine Gesundheitsreform im Sinne der ganzheitlichen Medizin. So wurde bei ihrem Stammtischgespräch in ihrer Eckkneipe der Fantasie keine Grenzen auferlegt. Jupp konnte sich letzten Monat selbst ein Bild von unserer Gesundheitsversorgung machen, nachdem er sich beim Pommes-Essen die Gabel aus Versehen ins Nasenloch gestoßen hatte. Er warf zunächst einen wachsamen Blick in die Runde, ob etwa wieder irgendwelche Hunde in seinem Umfeld zu finden waren. Ingo nutzte angesichts der Narbe an der Nase die Gelegenheit für einen aktuellen Ratschlag. Weiterlesen
(April 2024) Bereits vor zehn Jahren machte sich unser Duo Gedanken über eine Gesundheitsreform im Sinne der ganzheitlichen Medizin. So wurde bei ihrem Stammtischgespräch in ihrer Eckkneipe der Fantasie keine Grenzen auferlegt. Jupp konnte sich letzten Monat selbst ein Bild von unserer Gesundheitsversorgung machen, nachdem er sich beim Pommes-Essen die Gabel aus Versehen ins Nasenloch gestoßen hatte. Er warf zunächst einen wachsamen Blick in die Runde, ob etwa wieder irgendwelche Hunde in seinem Umfeld zu finden waren. Ingo nutzte angesichts der Narbe an der Nase die Gelegenheit für einen aktuellen Ratschlag. Weiterlesen
Arzneimittel mit KI entwickeln: „Es fehlen verlässliche rechtliche Vorgaben“
 (April 2024) Die Forschung an neuen Medikamenten ist ein teures und langwieriges Unterfangen. Bis zur Zulassung eines Arzneimittels dauert es etwa zwölf Jahre bei durchschnittlichen Gesamtkosten von etwa 2,8 Milliarden US-Dollar. Künstliche Intelligenz (KI) kann die Entwicklung von Arzneimitteln beschleunigen. Weiterlesen
(April 2024) Die Forschung an neuen Medikamenten ist ein teures und langwieriges Unterfangen. Bis zur Zulassung eines Arzneimittels dauert es etwa zwölf Jahre bei durchschnittlichen Gesamtkosten von etwa 2,8 Milliarden US-Dollar. Künstliche Intelligenz (KI) kann die Entwicklung von Arzneimitteln beschleunigen. Weiterlesen
Digital Deep Dive DMEA
 (April 2024) Die DMEA ist erwachsen geworden! Auch wenn sie unter dem aktuellen Namen noch nicht so viele Jahre agiert: Die Messe Berlin hat genau das richtige Konzept gefunden. Denn zählt man die ehemaligen Vor-Messen conhIT (Connecting Healthcare IT) und ITeG (Informationstechnologie im Gesundheitswesen, Frankfurt, ab 2003) dazu, sind die 21 Jahre – die ehemalige Volljährigkeit – mittlerweile erreicht. Weiterlesen
(April 2024) Die DMEA ist erwachsen geworden! Auch wenn sie unter dem aktuellen Namen noch nicht so viele Jahre agiert: Die Messe Berlin hat genau das richtige Konzept gefunden. Denn zählt man die ehemaligen Vor-Messen conhIT (Connecting Healthcare IT) und ITeG (Informationstechnologie im Gesundheitswesen, Frankfurt, ab 2003) dazu, sind die 21 Jahre – die ehemalige Volljährigkeit – mittlerweile erreicht. Weiterlesen
Jetzt ausgeschrieben: Forschungsförderpreis Patientensicherheit
 (April 2024) Die Deutsche Interdisziplinäre Vereinigung für Intensiv- und Notfallmedizin (DIVI) und Philips schreiben gemeinsam den Forschungsförderpreis Patientensicherheit aus. Der thematische Fokus der Auszeichnung soll die Bedeutsamkeit von Sicherheit für Patienten und Mitarbeitende im Gesundheitswesen unterstreichen. Weiterlesen
(April 2024) Die Deutsche Interdisziplinäre Vereinigung für Intensiv- und Notfallmedizin (DIVI) und Philips schreiben gemeinsam den Forschungsförderpreis Patientensicherheit aus. Der thematische Fokus der Auszeichnung soll die Bedeutsamkeit von Sicherheit für Patienten und Mitarbeitende im Gesundheitswesen unterstreichen. Weiterlesen
Virtueller Hautkontakt – Smarte Textilien machen Berührungen spürbar
 (April 2024) Smarte Textilien sollen ermöglichen, auch vom Körpergefühl her in die virtuelle Realität einzutauchen und Berührungen am eigenen Leib zu spüren. Eine hauchdünne Folie, die Berührungsempfindungen übertragen kann, macht dabei Stoffe zur zweiten, virtuellen Haut. Schwer kranken Kindern in Isolierstationen soll sie die Körpernähe ihrer Eltern bei computersimulierten Besuchen spürbar machen: Sie soll ihr Streicheln fühlbar übertragen. Weiterlesen
(April 2024) Smarte Textilien sollen ermöglichen, auch vom Körpergefühl her in die virtuelle Realität einzutauchen und Berührungen am eigenen Leib zu spüren. Eine hauchdünne Folie, die Berührungsempfindungen übertragen kann, macht dabei Stoffe zur zweiten, virtuellen Haut. Schwer kranken Kindern in Isolierstationen soll sie die Körpernähe ihrer Eltern bei computersimulierten Besuchen spürbar machen: Sie soll ihr Streicheln fühlbar übertragen. Weiterlesen
Handlungsempfehlungen für Forschungseinrichtungen in der Intensiv- und Notfallmedizin veröffentlicht (GDNG)
 (April 2024) Mit dem in Kraft getretenen Gesundheitsdatennutzungsgesetz (GDNG) wurde eine bundeseinheitliche Rechtsgrundlage für Verbundforschungsprojekte geschaffen, die vor allem in der Intensiv- und Notfallmedizin für die Qualitätssicherung sowie Steuerung von Prozessen und Ressourcen von großer Bedeutung ist. Weiterlesen
(April 2024) Mit dem in Kraft getretenen Gesundheitsdatennutzungsgesetz (GDNG) wurde eine bundeseinheitliche Rechtsgrundlage für Verbundforschungsprojekte geschaffen, die vor allem in der Intensiv- und Notfallmedizin für die Qualitätssicherung sowie Steuerung von Prozessen und Ressourcen von großer Bedeutung ist. Weiterlesen
Studie: Belastung für Ärzteschaft anhaltend hoch, Abbau Patientenstau verzögert sich

(April 2024) Die anhaltende Krise im Gesundheitswesen schlägt sich auf die Psyche der Ärzteschaft in ganz Europa nieder, sagt eine Studie, in der 600 Fachärzte in den Bereichen Onkologie und Chirurgie zur aktuellen Arbeitssituation europaweit befragt wurden. Demnach wirkt die Pandemie noch nach, denn die psychische Belastung hat sich bei den Befragten auch 2023 nicht verringert – sie liegt immer noch auf einem ähnlich hohen Niveau wie in den Erhebungsjahren 2021 und 2022. Weiterlesen
Positionspapier zur Europawahl: Eigener Gesundheitsausschuss im Europäischen Parlament
 (April 2024) Unter dem Titel „Medizintechnik-Standort Europa stärken“ ist für den Medizintechnik-Verband BVMed wichtig, dass Europa Lehren aus der Corona-Pandemie zieht, die Resilienz des Gesundheitssystems stärkt und damit die medizinische Versorgung krisenfest gestaltet. Weiterlesen
(April 2024) Unter dem Titel „Medizintechnik-Standort Europa stärken“ ist für den Medizintechnik-Verband BVMed wichtig, dass Europa Lehren aus der Corona-Pandemie zieht, die Resilienz des Gesundheitssystems stärkt und damit die medizinische Versorgung krisenfest gestaltet. Weiterlesen
NIS-2: Diese 8 Sofortmaßnahmen sollten Verantwortliche im Gesundheitssektor jetzt ergreifen
 (April 2024) Mit NIS-2 soll sich das IT-Sicherheitsniveau EU-weit erhöhen. Rechtliche Vorgaben sind im Gesundheitssektor nicht neu, jedoch werden mit der NIS-2-Direktive IT-Sicherheitsmaßnahmen für mehr Organisationen verpflichtend. Auch Krankenhäuser stehen vor zeitlichen und organisatorischen Herausforderungen. Diese acht NIS-2-Sofortmaßnahmen helfen Verantwortlichen bei der Umsetzung. Weiterlesen
(April 2024) Mit NIS-2 soll sich das IT-Sicherheitsniveau EU-weit erhöhen. Rechtliche Vorgaben sind im Gesundheitssektor nicht neu, jedoch werden mit der NIS-2-Direktive IT-Sicherheitsmaßnahmen für mehr Organisationen verpflichtend. Auch Krankenhäuser stehen vor zeitlichen und organisatorischen Herausforderungen. Diese acht NIS-2-Sofortmaßnahmen helfen Verantwortlichen bei der Umsetzung. Weiterlesen
Symposium „Daten statt raten“ vermittelt konkrete Ansätze und Vorteile von Simulation für Medizintechnik
 (April 2024) Beim Symposium „Daten statt raten“ zeigten Entwicklungen und Best Practices aus Industrie und Forschung, dass Simulation der Medizintechnik bereits sehr reale Chancen bietet, ihre Wettbewerbsfähigkeit auszubauen – und den Patienten ungeahnte Perspektiven eröffnet. Weiterlesen
(April 2024) Beim Symposium „Daten statt raten“ zeigten Entwicklungen und Best Practices aus Industrie und Forschung, dass Simulation der Medizintechnik bereits sehr reale Chancen bietet, ihre Wettbewerbsfähigkeit auszubauen – und den Patienten ungeahnte Perspektiven eröffnet. Weiterlesen
Deutscher Nachhaltigkeitspreis Gesundheit: Leuchttürme gelungener Transformation gesucht
 (März 2024) Ab sofort sind Bewerbungen für den neuen Deutschen Nachhaltigkeitspreis Gesundheit möglich. Die Bewerbungsfrist endet am 31. Mai. Der Preis würdigt Projekte, die die Transformation des Gesundheitswesens in Deutschland zu mehr Nachhaltigkeit vorantreiben. Weiterlesen
(März 2024) Ab sofort sind Bewerbungen für den neuen Deutschen Nachhaltigkeitspreis Gesundheit möglich. Die Bewerbungsfrist endet am 31. Mai. Der Preis würdigt Projekte, die die Transformation des Gesundheitswesens in Deutschland zu mehr Nachhaltigkeit vorantreiben. Weiterlesen
Neues Zentrum für Synthetische Genomik
 (März 2024) Die Anwendung und Entwicklung neuer Technologien der DNA-Synthese voranzutreiben, um den Weg für die Herstellung ganzer künstlicher Genome zu ebnen – das ist das Ziel eines neuen interdisziplinären Zentrums, das an der Universität Heidelberg, dem Karlsruher Institut für Technologie (KIT) und der Johannes Gutenberg-Universität Mainz (JGU) entsteht. Weiterlesen
(März 2024) Die Anwendung und Entwicklung neuer Technologien der DNA-Synthese voranzutreiben, um den Weg für die Herstellung ganzer künstlicher Genome zu ebnen – das ist das Ziel eines neuen interdisziplinären Zentrums, das an der Universität Heidelberg, dem Karlsruher Institut für Technologie (KIT) und der Johannes Gutenberg-Universität Mainz (JGU) entsteht. Weiterlesen
Jeder Vierte braucht ein medizinisches Hilfsmittel (HMVZ)
 (März 2024) Krücken, Einlagen, Orthesen und Co.: Wie SBK-Zahlen zeigen, braucht jeder Vierte mindestens einmal pro Jahr ein Hilfsmittel. Mit zunehmendem Alter steigt der Bedarf. Das Hilfsmittelverzeichnis gibt einen Überblick über Hilfsmittel, die unter die Leistungspflicht der GKV fallen. Weiterlesen
(März 2024) Krücken, Einlagen, Orthesen und Co.: Wie SBK-Zahlen zeigen, braucht jeder Vierte mindestens einmal pro Jahr ein Hilfsmittel. Mit zunehmendem Alter steigt der Bedarf. Das Hilfsmittelverzeichnis gibt einen Überblick über Hilfsmittel, die unter die Leistungspflicht der GKV fallen. Weiterlesen
Q.ANT und Fraunhofer IPA gründen Kompetenz-Zentrum
 (März 2024) Im März haben das Fraunhofer-Institut für Produktionstechnik und Automatisierung IPA und das Technologieunternehmen Q.ANT einen Vertrag zur Gründung des Kompetenz-Zentrums Mensch-Maschine-Schnittstelle unterzeichnet. Weiterlesen
(März 2024) Im März haben das Fraunhofer-Institut für Produktionstechnik und Automatisierung IPA und das Technologieunternehmen Q.ANT einen Vertrag zur Gründung des Kompetenz-Zentrums Mensch-Maschine-Schnittstelle unterzeichnet. Weiterlesen
Neue Möglichkeit, die Entscheidung zur Organ- und Gewebespende festzuhalten
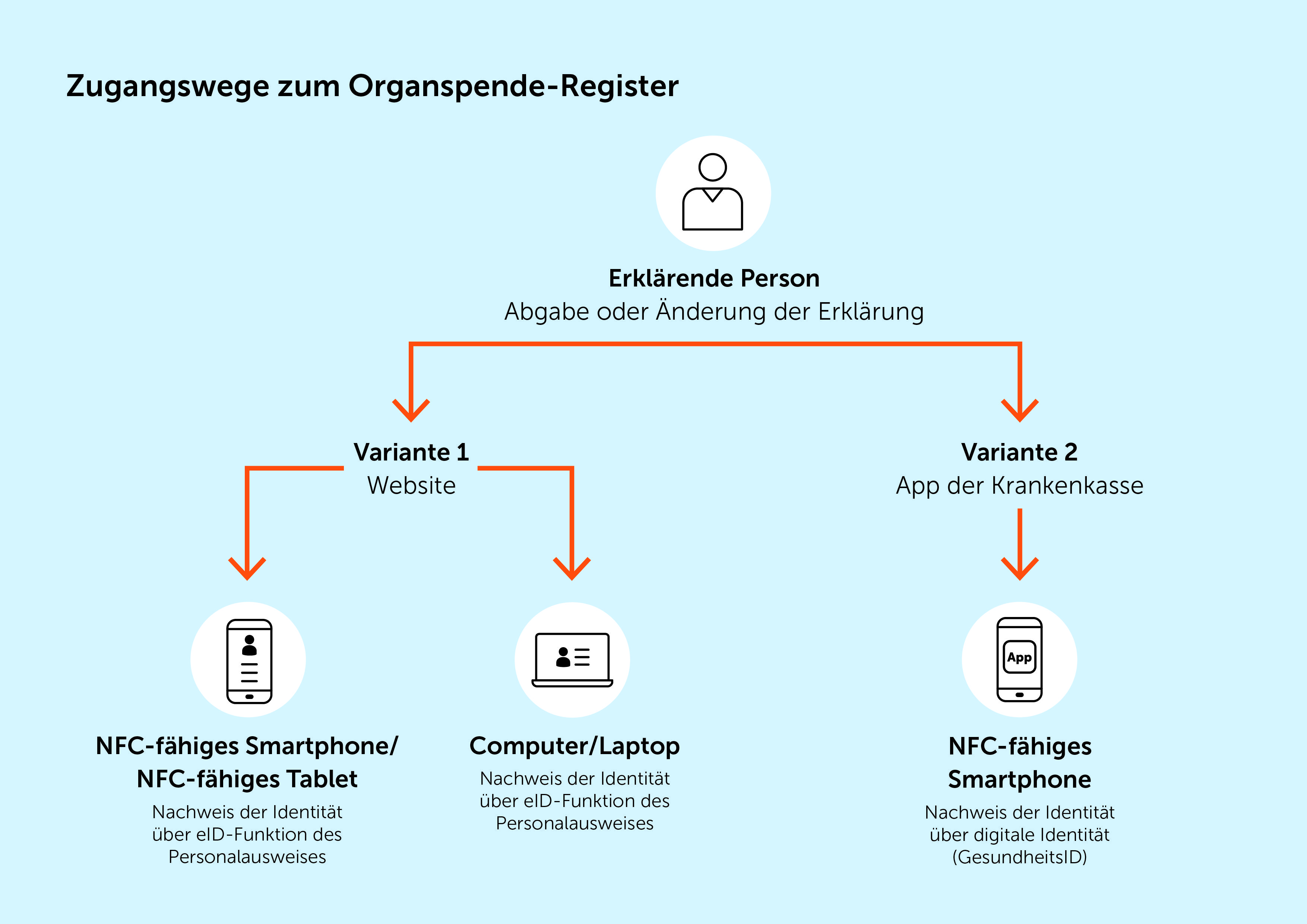 (März 2024) Das Register für Erklärungen zur Organ- und Gewebespende – kurz Organspende-Register – nimmt schrittweise seinen Betrieb auf. Zusätzlich zum Organspendeausweis und der Patientenverfügung steht damit eine digitale Möglichkeit zur Verfügung, die persönliche Entscheidung zur Organ- und Gewebespende festzuhalten. Weiterlesen
(März 2024) Das Register für Erklärungen zur Organ- und Gewebespende – kurz Organspende-Register – nimmt schrittweise seinen Betrieb auf. Zusätzlich zum Organspendeausweis und der Patientenverfügung steht damit eine digitale Möglichkeit zur Verfügung, die persönliche Entscheidung zur Organ- und Gewebespende festzuhalten. Weiterlesen
Smarte Blutdruckmessgeräte auswählen und anwenden
 (März 2024) Smarte Blutdruckmessgeräte erleichtern das Messen im Alltag und die Auswertung der Ergebnisse. Auswahl des Gerätes nach individuellen Bedürfnissen. Zertifizierung als Medizinprodukt gewährleistet hohe Messgenauigkeit. Bei App-Nutzung auf Cybersicherheit achten. TÜV-Verband gibt Tipps zum Kauf und Gebrauch von Blutdruckmessgeräten. Weiterlesen
(März 2024) Smarte Blutdruckmessgeräte erleichtern das Messen im Alltag und die Auswertung der Ergebnisse. Auswahl des Gerätes nach individuellen Bedürfnissen. Zertifizierung als Medizinprodukt gewährleistet hohe Messgenauigkeit. Bei App-Nutzung auf Cybersicherheit achten. TÜV-Verband gibt Tipps zum Kauf und Gebrauch von Blutdruckmessgeräten. Weiterlesen
Preis für Innovation in der Medizintechnik
 (März 2024) Alle zwei Jahre prämiert die deutsche Gesellschaft für Biomedizinische Technik im VDE in Kooperation mit der Stiftung Familie Klee herausragende Lösungen für medizinische Fragestellungen. Der Preis ist mit 10.000 EUR dotiert und wird mit einer Urkunde ausgezeichnet. Weiterlesen
(März 2024) Alle zwei Jahre prämiert die deutsche Gesellschaft für Biomedizinische Technik im VDE in Kooperation mit der Stiftung Familie Klee herausragende Lösungen für medizinische Fragestellungen. Der Preis ist mit 10.000 EUR dotiert und wird mit einer Urkunde ausgezeichnet. Weiterlesen
MDR-Debatte im EU-Parlament: Lösungen schnellstmöglich vorantreiben
 (März 2024) Die klaren Aussagen in der Debatte des Europäischen Parlaments (EP) zu notwendigen Verbesserungen der EU-Medizinprodukte-Verordnung (MDR) sind zu begrüßen. „Die Debatte zeigt deutlich…, dass die MDR über das Ziel hinausgeschossen ist und dringend nachgebessert werden muss. Auch die Abschaffung der Rezertifizierung von Bestandsprodukten ist ein gutes Signal“, erklärt der BVMed. Weiterlesen
(März 2024) Die klaren Aussagen in der Debatte des Europäischen Parlaments (EP) zu notwendigen Verbesserungen der EU-Medizinprodukte-Verordnung (MDR) sind zu begrüßen. „Die Debatte zeigt deutlich…, dass die MDR über das Ziel hinausgeschossen ist und dringend nachgebessert werden muss. Auch die Abschaffung der Rezertifizierung von Bestandsprodukten ist ein gutes Signal“, erklärt der BVMed. Weiterlesen
